
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Hydrogénuhličitan | |
 | |
 | |
| Všeobecné vlastnosti | |
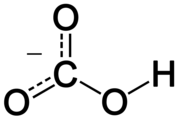
| Sumárny vzorec | HCO3- |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 61,0168 g/mol |
| Ďalšie informácie | |
| Číslo CAS | 71-52-3 |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
Hydrogénuhličitan[1] alebo hydrogenuhličitan[1][2] (staršie hydrouhličitan[1], v lekárstve občas bikarbonát) je jeden z aniónov kyseliny uhličitej. Tento anorganický anión vzniká deprotonáciou kyseliny uhličitej. Je to polyatómový anión, ktorého vzorec je HCO3-. Soli obsahujúce tento anión sa označujú ako hydrogénuhličitany.
Hydrogénuhličitan má dôležitú biochemickú úlohu ako fyziologický tlmivý roztok.[3]
Chemické vlastnosti
Hydrogénuhličitanový anión sa skladá z jedného atómu uhlíka, na ktorý sú naviazané tri kyslíkové atómy v trigonálne planárnom usporiadaní. Na jeden z týchto kyslíkov je naviazaný vodíkový atóm. Tento anión je izoelektronický s kyselinou dusičnou, HNO3. Formálny náboj hydrogénuhličitanového aniónu je mínus jedna a je amfiprotický, takže má kyslé i zásadité vlastnosti. Je to konjugovaná zásada kyseliny uhličitej a zároveň konjugovaná kyselina uhličitanového aniónu, čo vyjadrujú nasledujúce rovnovážne rovnice:[chýba zdroj
- H2CO3 + 2 H2O ↔ HCO3- + H3O+ + H2O ↔ CO32- + 2 H3O+
- CO32- + 2 H2O ↔ HCO3- + H2O + OH− ↔ H2CO3 + 2 OH−
Soli hydrogénuhličitanu vznikajú spojením kladne nabitého iónu na záporne nabitý kyslíkový atóm tohto iónu, čim vzniká iónová zlúčenina. Mnohé hydrogénuhličitany sú rozpustné vo vode pri štandardnej teplote a tlaku. Hydrogénuhličitan sodný prispieva k množstvu rozpustených minerálov vo vode, čo je bežný parameter pre meranie kvality vody.[4]
Fyziologický význam
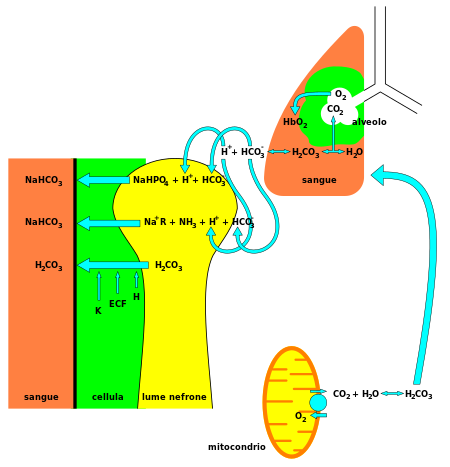
Hydrogénuhličitan je dôležitou zložkou tlmivého roztoku ľudského tela,[3] vďaka čomu sa udržiava acidobázická homeostáza (približne konštantné pH). Celkom 70 až 75 % oxidu uhličitého v tele sa premení na kyselinu uhličitú (H2CO3), konjugovanú kyselinu HCO3-, na ktorý sa môže rýchlo premeniť.
Hydrogénuhličitan, voda, vodíkové ióny a oxid uhličitý tvoria tlmivý roztok, pričom kyselina uhličitá pôsobí ako reakčný intermediát. Tento tlmivý roztok sa udržiava pri nestálej rovnováhe[3] a poskytuje rýchlu odpoveď a obranu na zmenu pH smerom ku kyslému i zásaditému prostrediu. To je veľmi dôležité hlavne pri ochrane tkanív centrálnej nervovej sústavy, kde zmena pH výrazne mimo normálneho rozsahu môže mať katastrofálne následky (pozri acidóza a alkalóza).
Hydrogénuhličitan je naviac dôležitý v tráviacom trakte. Zvyšuje vnútorné pH žalúdka po tom, čo veľmi kyslé žalúdočné šťavy dokončili trávenie potravy. Hydrogénuhličitan takisto reguluje pH v tenkom čreve. Vylučuje sa z pankreasu v reakcii na hormón sekretín a neutralizuje kyslú tráveninu vystupujúcu zo žalúdku do dvanástnika.[5]
Hydrogénuhličitan v prostredí
Hydrogénuhličitan je hlavnou formou rozpusteného anorganického uhlíka v slanej vode[6] a väčšine sladkých vôd. Kvôli tomu je dôležitý v cykle uhlíka.
V sladkovodnej ekológii sa následkom silnej fotosyntetickej aktivity sladkovodných rastlín cez deň vylučuje plynný kyslík do vody a zároveň s tým vznikajú hydrogénuhličitanové anióny. Kvôli tomu dochádza k zvýšeniu pH, až kým sa v konkrétnych prípadoch táto zásaditosť nestane toxickou pre niektoré organizmy alebo sa kvôli tomu nestanú iné látky toxickými, napríklad amoniak. V tme, keď fotosyntéza neprebieha, dochádza k vzniku oxidu uhličitého respiračnými procesmi, takže nevznikajú nové ióny hydrogénuhličitanu a pH rýchlo klesá.[chýba zdroj
Použitie v potravinárstve
Najbežnejšou soľou s hydrogénuhličitanovým anión je hydrogénuhličitan sodný, NaHCO3, ktorý je bežné známy ako sóda bikarbóna. Keď sa zahreje alebo vystaví kyseline, napríklad kyseline octovej (ktorá je prítomná v octe), hydrogénuhličitanový anión sa rozkladá a vzniká z neho oxid uhličitý. Preto sa používa ako kypriaca látka do pečenia.[7]
Hydrogénuhličitan amónny sa používa pri výrobe sušienok na trávenie.[chýba zdroj
Diagnostika
V diagnostickej medicíne je hladina hydrogénuhličitanu v krvi jedným zo sledovaných parametrov, ktoré naznačujú acidobázickú rovnováhu v tele. Meria sa spolu s oxidom uhličitým, chloridmi, draslíkom a sodíkom, čím sa zisťuje hladina elektrolytov v krvi.[8] Nerovnováha môže poukazovať na acidózu alebo alkalózu.

Zlúčeniny s hydrogénuhličitanovým aniónom
Medzi hydrogénuhličitany patria napríklad:
- Hydrogénuhličitan sodný
- Hydrogénuhličitan draselný
- Hydrogénuhličitan cézny
- Hydrogénuhličitan horečnatý
- Hydrogénuhličitan vápenatý
- Hydrogénuhličitan amónny
Referencie
- ↑ a b c hydrogénuhličitan | Jazyková poradňa | SME.sk . jazykovaporadna.sme.sk, . Dostupné online.
- ↑ hydrogenuhličitany. In: Encyclopaedia Beliana. 1. vyd. Bratislava : Encyklopedický ústav SAV; Veda, 2010. 686 s. ISBN 978-80-970350-0-6. Zväzok 6. (His – Im), s. 369.
- ↑ a b c Clinical correlates of pH levels: bicarbonate as a buffer . Biology.arizona.edu, October 2006. Dostupné online. Archivované 2015-05-31 z originálu.
- ↑ GEOR, Raymond J.; COENEN, Manfred; HARRIS, Pat. Equine Applied and Clinical Nutrition: Health, Welfare and Performance. : Elsevier Health Sciences, 31 January 2013. ISBN 978-0-7020-5418-1. S. 90. (po anglicky)
- ↑ Berne & Levy, Principles of Physiology
- ↑ The chemistry of ocean acidification : OCB-OA . Woods Hole Oceanographic Institution, 24 September 2012. Dostupné online. Archivované 2017-05-19 z originálu. (po anglicky)
- ↑ Jaký je rozdíl mezi práškem do pečiva a jedlou sodou? . 2018-05-03, . Dostupné online. (po česky)
- ↑ Acid Base Balance (page 3) Archivované 2002-06-13 na Wayback Machine
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Bicarbonate na anglickej Wikipédii.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk
