
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9

Stredná kvadratická rýchlosť[1][2] je taká rýchlosť, akú by museli mať všetky častice ideálneho plynu, aby ich celková kinetická energia bola taká istá, aká je ich skutočná celková kinetická energia s reálnymi rýchlosťami. Skutočná celková kinetická energia je súčtom kinetických energií všetkých častíc plynu, keď ich reálne rýchlosti sú rôzne. Je to štatistická veličina.
Rovnica pre strednú kvadratickú rýchlosť
Celkovú kinetickú energiu Ek (J) pre N častíc ideálneho plynu, s rýchlosťou i-tej častice vi (m/s) a s hmotnosťou jednej častice m0 (kg) vypočítame ako súčet kinetických energií všetkých N častíc, podľa vzorca:
Reálne kvadratické rýchlosti častíc : môžeme nahradiť strednou kvadratickou rýchlosťou vs:
Pre kinetickú energiu jednej častice plynu E0 (J) so strednou kvadratickou rýchlosťou vs (m/s) môžeme písať:
Pretože kinetickú energiu ideálneho plynu je možné vyjadriť aj pomocou Boltzmanovej konšatnty a teploty plynu T (K):[3]
tak strednú kvadratickú rýchlosť môžeme vyjadriť ako:
- .
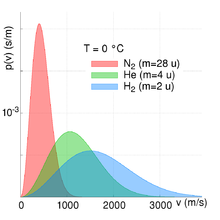
Pozoruhodné na tomto vzorci je, že stredná kvadratická rýchlosť závisí okrem hmotnosti častice len na teplote a nie na objeme alebo tlaku, tzn. je úplne jedno, koľko častíc je v danej nádobe. Pri danej teplote majú častice toho istého plynu vždy rovnakú strednú kvadratickú rýchlosť. Hmotnosť jednej častice m0 v kilogramoch získame ako podiel molárnej hmotnosti a Avogadrovej konštanty.
Stredná a najpravdepodobnejšia rýchlosť
Najpravdepodobnejšia rýchlosť vn nie je totožná so strednou rýchlosťou vm, ani so strednou kvadratickou rýchlosťou vs.[3]
Stredná kinetická energia
Rôzne plyny pri rovnakej teplote majú rovnakú strednú kinetickú energiu pohybu molekúl.[4] Kinetickú energiu môžeme vyjadriť aj v elektrónvoltoch jednoduchým prevedením podľa vzorca: 1 eV = 1,602 176 53 E−19 J.
| Plyn | Mólová hmotnosť | pri 100 K | pri 300 K | pri 800 K | pri 1500 K |
|---|---|---|---|---|---|
| atomárny vodík H |
1 g/mol | 1579 m/s 0,01 eV |
2735 m/s 0,04 eV |
4467 m/s 0,1 eV |
6117 m/s 0,19 eV |
| vodík H2 | 2 g/mol | 1117 m/s 0,01 eV |
1934 m/s 0,04 eV |
3158 m/s 0,1 eV |
4325 m/s 0,19 eV |
| Hélium He | 4 g/mol | 790 m/s 0,01 eV |
1368 m/s 0,04 eV |
2233 m/s 0,1 eV |
3058 m/s 0,19 eV |
| Dusík N2 | 28 g/mol | 298 m/s 0,01 eV |
571 m/s 0,04 eV |
844 m/s 0,1 eV |
1156 m/s 0,19 eV |
Pozri aj
Referencie
- ↑ Střední kvadratická rychlost, REICHL, Jaroslav; VŠETIČKA, Martin. Encyklopedie fyziky . fyzika.jreichl.com, . Dostupné online. (po česky)
- ↑ Stredná kvadratická rýchlosť, stavová rovnica gymsnv.sk, . Dostupné online.
- ↑ a b Maxwellovo rozdelenie molekúl podľa rýchlostí BALLO, Peter. STUonline . kf-lin.elf.stuba.sk, . Dostupné online.
- ↑ Teplota a vnútorná energia plynu, BALLO, Peter. STUonline . kf-lin.elf.stuba.sk, . Dostupné online.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk









