
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Chlorid antimoničný | |
|---|---|
 Strukturní vzorec | |
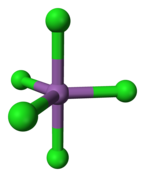 Model chloridu antimoničného | |
| Obecné | |
| Systematický název | chlorid antimoničný |
| Anglický název | Antimony(V) pentachloride |
| Německý název | Antimon(V)-chlorid |
| Sumární vzorec | SbCl5 |
| Vzhled | bezbarvá nebo červenožlutá kapalina |
| Identifikace | |
| Registrační číslo CAS | 7647-18-9 |
| PubChem | 24294 |
| SMILES | ..... |
| InChI | InChI=1S/5ClH.Sb/h5*1H;/q;;;;;+3/p-5 |
| Číslo RTECS | CC5075000 |
| Vlastnosti | |
| Molární hmotnost | 299,01 g/mol |
| Teplota tání | 2,8 °C |
| Teplota varu | 140 °C (rozklad od 106 °C) |
| Hustota | 2,336 g/cm3 (20 °C) 2,36 g/cm3 (25 °C) |
| Index lomu | 1,59255 |
| Rozpustnost v polárních rozpouštědlech | alkoholy, kyselina chlorovodíková, sirouhlík |
| Rozpustnost v nepolárních rozpouštědlech | tetrachlormethan |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
Některá data mohou pocházet z datové položky. | |
Chlorid antimoničný je anorganická sloučenina s vzorcem SbCl5. Jedná se o bezbarvou kapalinu, která je ale často zbarvena do žluta. V přítomnosti vlhkosti hydrolyzuje za uvolnění chlorovodíku.
Příprava
Připravuje se reakcí plynného chloru s chloridem antimonitým.
- SbCl3 + Cl2 → SbCl5
Reakce
Chlorid antimoničný hydrolyzuje za vzniku kyseliny chlorovodíkové a oxidu-chloridu antimoničného.
- SbCl5 + H2O → SbOCl3 + 2 HCl
Tuto reakci lze potlačit vysokou koncentrací chloridů, pak vzniká komplexní anion hexachloroantimoničný:
- SbCl5 + Cl− → SbCl -
6
Vytváří řadu aduktů s Lewisovými bázemi. Má také silné oxidační vlastnosti.[2]
Využití
Využívá se jako katalyzátor polymerizací a na chloraci organických sloučenin.
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Antimony pentachloride na anglické Wikipedii.
- ↑ a b Antimony pentachloride. pubchem.ncbi.nlm.nih.gov . PubChem . Dostupné online. (anglicky)
- ↑ CONNELLY, Neil G.; GEIGER, William E. Chemical Redox Agents for Organometallic Chemistry. Chemical Reviews. 1996-1, roč. 96, čís. 2, s. 877–910. Dostupné online . ISSN 0009-2665. DOI 10.1021/cr940053x. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu chlorid antimoničný na Wikimedia Commons
Obrázky, zvuky či videa k tématu chlorid antimoničný na Wikimedia Commons
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk


