A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Bifenyl | |||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||
| Sumárny vzorec | C12H10 | ||||||||||||||||||||||||||||||||
| Synonymá | 1,1'-bifenyl, difenyl, fenylbenzén, E 230 | ||||||||||||||||||||||||||||||||
| Vzhľad | biele až svetložlté kryštály | ||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 154,212 g·mol−1 | ||||||||||||||||||||||||||||||||
| Teplota topenia | 69,2 °C[1] | ||||||||||||||||||||||||||||||||
| Teplota varu | 255 °C[1] | ||||||||||||||||||||||||||||||||
| Hustota | 1,04 g/cm3[1] | ||||||||||||||||||||||||||||||||
| Rozpustnosť | 4,45 mg/dm3 (vo vode)[1] | ||||||||||||||||||||||||||||||||
| Teplota vzplanutia | 113 °C[1] | ||||||||||||||||||||||||||||||||
| Teplota vznietenia | 540 °C[1] | ||||||||||||||||||||||||||||||||
| Medze výbušnosti | 0,6 – 5,8 %[2] | ||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||
| Číslo CAS | 92-52-4 | ||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||
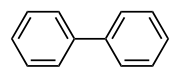
Bifenyl (niekedy aj difenyl, fenylbenzén; systematický názov: 1,1'-bifenyl) je aromatická organická zlúčenina. Za normálnych podmienok ide o pevnú látku, ktorá tvorí biele kryštály. Vyznačuje sa príjemnou vôňou. Je prakticky nerozpustný vo vode, dá sa však rozpustiť v bežne dostupných organických rozpúšťadlách. Z hľadiska štruktúry ide vlastne o 2 benzénové jadrá spojené jednoduchou väzbou. Alkyl a funkčná skupina odvodené od bifenylu sa nazývajú bifenylyl a bifenylová skupina.[3]
Výroba
Bifenyl sa prirodzene vyskytuje v surovej rope a uhoľnom dechte. Z týchto zdrojov sa dá oddeliť destiláciou.
Priemyselne vzniká ako vedľajší produkt pri výrobe benzénu, pomocou dealkylácie toluénu, pri nasledujúcej reakcii:
Zámerne sa priemyselne vyrába pomocou oxidačnej dehydrogenácie benzénu. Tá prebieha nasledovne:
2 C6H6 + 0,5 O2 → C12H10 + H2O
V laboratóriu sa dá pripraviť z brómbenzénu, z ktorého sa reakciou s horčíkom pripraví grignardov reaktant, fenylmagnéziumbromid. Ten po pridaní brómbenzénu reaguje a vzniká bifenyl.
Využitie
Chemický priemysel
Pretože bifenyl nemá na sebe naviazané žiadne funkčné skupiny ani iné substituenty je pomerne málo reaktívny. Využíva sa však ako surovina na výrobu polychlórovaných bifenylov, ktoré kedysi boli široko používané elektricky izolujúce teplovodné kvapaliny a pesticídy.[4]
Potravinársky priemysel
Bifenyl zabraňuje rastu húb a plesní a preto sa využíva aj ako konzervačná látka s E číslom E 230. Používa sa väčšinou v citrusových plodoch a najmä pri ich prevoze. Používanie na potravinárske účely je však v štátoch EÚ zakázané.
Ostatné
V zmesi s difenyléterom (tiež tuhá látka) vytvára eutektickú zmes a je kvapalný. Táto zmes sa využíva ako teplovodná látka na prenos tepla a je chemicky stabilná až do 400 °C.
Referencie
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Acesulfám draselný
Anoxomer
Benzaldehyd
Bifenyl
Brilantná čierna BN
Brilantná modrá FCF
Chlorid horečnatý
Chlorid vápenatý
Citrát železito-amónny
Citrát amónno-železitý
Citrát trivápenatý
Difosforečnan
Dihydrogencitrát vápenatý
Disodné ribonukleotidy
Dusičnan sodný
Emulgátor
Erytorban sodný
Flavínmononukleotid
Glutaman sodný
Hexametyléntetraamín
Hinokitiol
Hydrogencitrát vápenatý
Inozinát sodný
Jodid draselný
Jodid vápenatý
Kaolín
Karagén
Kurkuma pravá
Kvasinka
Kyselina adipová
Kyselina erytorbová
Kyselina jablčná
Kyselina jantárová
Kyselina octová
Kyselina propiónová
Manitol
Mliečnan sodný
Oxid chloričitý
Peroxodisíran draselný
Polyetylénglykol
Propán-1,2-diol
Propionát draselný
Propionát sodný
Propionát vápenatý
Síran amónny
Síran draselno-hlinitý
Sorbát
Sorban draselný
Sorbitol
Sukralóza
Trietylcitrát
Zoznam prídavných látok v potravinách
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk