A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Kyselina benzoová | |||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||
| Sumárny vzorec | C6H5COOH | ||||||||||||||||||
| Vzhľad | bezfarebná kryštalická látka | ||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||
| Molárna hmotnosť | 122,123 g·mol-1 | ||||||||||||||||||
| Teplota topenia | 122 °C | ||||||||||||||||||
| Teplota varu | 250 °C | ||||||||||||||||||
| Hustota | 1265,9 g·dm3 | ||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||
| Merná tepelná kapacita | 146,7 J·mol-1·K-1 | ||||||||||||||||||
| |||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||
| Číslo CAS | 65-85-0 | ||||||||||||||||||
| EINECS číslo | 200-618-2 | ||||||||||||||||||
| Číslo RTECS | DG0875000 | ||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||
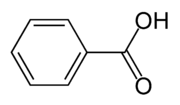
Kyselina benzoová (správne kyselina benzénkarboxylová, vzácnejšie kyselina fenylmravčia) je tuhá bezfarebná kryštalická látka s racionálnym vzorcom C6H5COOH. Je najjednoduchšou aromatickou karboxylovou kyselinou. V potravinárstve má priradené E číslo E210.
Vlastnosti
Fyzikálne vlastnosti
Kyselina benzoová tvorí pri normálnych podmienkach bezfarebné kryštály bez zápachu. Teplota topenia je 122,4 °C a vrie pri 249 °C. Pri vyšších teplotách (nad 100 °C) sublimuje. Vo vode sa pri 20 °C rozpúšťa len mierne (3,4 g/l vody), rozpustnosť možno zvýšiť prídavkom silnej zásady (napr. NaOH) resp. miernym zahriatím.
- Hustota: 1321 kg/m3
- Mólová hmotnosť: 122,12 g/mol
- pH: 3,1–3,3 (10 g/l vody)
- Tlak pár: 1,3 Pa
- Medza výbušnosti: 1,4 obj. %
Chemické vlastnosti
Kyselina benzoová patrí v rámci organických kyselín medzi stredne silné kyseliny (pKa = 4,17). Jej vyššiu kyslosť oproti alifatickým analógom spôsobuje stabilizačné pôsobenie aromatického jadra po odštiepení protónu z karboxylovej skupiny.
Kyselina benzoová poskytuje všetky reakcie charakteristické pre karboxylové kyseliny (napr. esterifikácia, tvorba solí, tvorba funkčných derivátov):
Na aromatickom jadre možno uskutočniť elektrofilné substitúcie, prebiehajú však ťažšie než na benzéne:
Použitie
Kyselina benzoová a jej soli (benzoan sodný, draselný, vápenatý) sú mierne toxické (LD50 ≈ 0,5 g/kg) a používajú sa ako konzervačné prísady (E210, E211, E212, E213). Konzervačný účinok spočíva v schopnosti kyseliny benzoovej inhibovať rast kvasiniek, baktérií a obzvlášť plesní. Kyselina benzoová sa používa na konzerváciu potravín kyslého charakteru (citrusové šťavy, sýtené nápoje). Doteraz sa vedú spory o zdravotnej nezávadnosti jej používania ako konzervačného prípravku.
Kyselina benzoová slúži aj ako dôležitá surovina pri výrobe fenolu, benzoylchloridu, dibenzoylperoxidu (iniciátor polymerizácie).
Výroba
Svetová ročná produkcia kyseliny benzoovej dosahuje 0,25 mil. ton. Priemyselne sa vyrába oxidáciou toluénu kyselinou dusičnou resp. vzdušným kyslíkom za prítomnosti kobaltnatých katalyzátorov alebo dekarboxyláciou kyseliny ftalovej.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Šelak
Žltá 2G
Žltá SY
Β-Kryptoxantín
Acesulfám draselný
Acetanhydrid
Aktívne uhlie
Amarant
Amoniak
Anoxomer
Antokyán
Argón
Aspartám
Bentonit
Benzoan sodný
Benzoylperoxid
Benzylalkohol
Betakarotén
Bifenyl
Brilantná čierna BN
Brilantná modrá FCF
Brilantná zelená BS
Bután
Celulóza (organická látka)
Chlór
Chlorid amónny
Chlorid cínatý
Chlorid draselný
Chlorid horečnatý
Chlorid vápenatý
Chlorofyl
Citrát trisodný
Citrát trivápenatý
Difosforečnan
Dihydrogéncitrát sodný
Dihydrogencitrát vápenatý
Dihydrogenfosforečnan sodný
Dusík
Dusičnan draselný
Dusičnan sodný
Dusitan sodný
Erytorban sodný
Etanol
Etylacetát
E číslo
Flavínmononukleotid
Flavoxantín
Glutaman sodný
Glycín
Glycerol
Hélium
Hexakyanoželeznatan draselný
Hexametyléntetraamín
Hliník
Hydrogéncitrát sodný
Hydrogénsíran sodný
Hydrogénuhličitan sodný
Hydrogencitrát vápenatý
Hydrogenfosforečnan vápenatý
Hydrogensíran draselný
Hydrogenvínan draselný
Hydroxid draselný
Hydroxid sodný
Hydroxid vápenatý
Inozinát sodný
Jodid draselný
Jodid vápenatý
Karagén
Karamel
Karmín
Karotén
Kyselina adipová
Kyselina askorbová
Kyselina benzoová
Kyselina chlorovodíková
Kyselina citrónová
Kyselina erytorbová
Kyselina fumarová
Kyselina glutámová
Kyselina jablčná
Kyselina jantárová
Kyselina mliečna
Kyselina mravčia
Kyselina octová
Kyselina propiónová
Kyselina sírová
Kyselina sorbová
Kyselina trihydrogenfosforečná
Kyselina vínna
Kyslík
Lanolín
Manitol
Metylpropán
Mliečnan sodný
Mravčan amónny
Mravčan vápenatý
Niacín
Octan sodný
Oxidy dusíka
Oxid chloričitý
Oxid dusný
Oxid horečnatý
Oxid kremičitý
Oxid siričitý
Oxid titaničitý
Oxid uhličitý
Oxid vápenatý
Pektín
Propán
Propionát draselný
Propionát sodný
Propionát vápenatý
Riboflavín
Sépiolit
Síran amónno-hlinitý
Síran amónny
Síran draselný
Síran draselno-hlinitý
Síran meďnatý
Síran sodný
Síran vápenatý
Sorban draselný
Sorbitol
Striebro
Sukralóza
Talk
Tartrazín
Tetracyklín
Tiosíran sodný
Trietylcitrát
Uhličitan železnatý
Uhličitan draselný
Uhličitan horečnatý
Uhličitan sodný
Uhličitan vápenatý
Vermikulit
Vodík
Zlato
Zoznam prídavných látok v potravinách
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk