A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9

Ligandy[1] alebo adendy[1] (niekedy označované ako L) sú v koordinačnej chémii atómy alebo atómové skupiny (t.j. ióny alebo molekuly) koordinované okolo centrálneho atómu komplexu koordinačnej zlúčeniny (čiže sú naň viazané koordinačnou väzbou[2]).[1][3] Spravidla sú to donory elektrónov, ktoré sa skladajú z nekovových atómov.[4] Ligandy sú teda spravidla Lewisove bázy.[4]
Klasifikácia
Existuje všeobecne veľké množstvo ligandov, ktoré je možné kategorizovať mnohými spôsobmi. Jeden zo spôsobov je napríklad podľa zložitosti molekuly:[4]
- monoatómové ligandy – ligandy zložené z jediného atómu, napríklad F- alebo S2-
- polyatómové monocentrické ligandy – ligandy, ktoré okrem väzbového atómu obsahujú len atómy viazané priamo na tento atóm, napríklad CN- alebo NO2-
- polyatómové polycentrické ligandy – zvyčajne veľké organické molekuly, ktoré obsahujú väčší počet atómov, napríklad étery (R2O) alebo alkylamíny (NR3)
Alternatívne je ligandy možné klasifikovať podľa ich náboja:[1]
- neutrálne ligandy, napríklad NH3 alebo H2O
- aniónové ligandy, napríklad OH- alebo Cl-
- katiónové ligandy, napríklad NO+
Chelácia
Niektoré ligandy sa môžu na centrálny atóm viazať viac než jednou väzbou, takže ďalším spôsobom kategorizácie môže byť počet väzieb, ktoré ligand tvorí. Z tohto hľadiska možno rozlišovať ligandy napríklad nasledovne:[4]
- monodentátne ligandy – tvoria len jednu väzbu, napríklad Cl- (tieto ligandy môžu tvoriť viac väzieb, ak sú prítomné v komplexoch s viac než jedným centrálnym atómom, vtedy vystupujú ako mostíkové atómy)
- bidentátne ligandy – tvoria dve väzby, napríklad etyléndiamín
- tridentátne ligandy – tvoria tri väzby, napríklad 1,4,7-trioxacyklononán
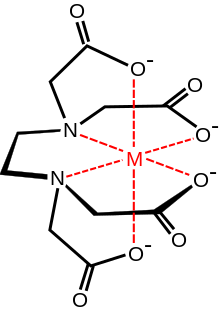
- polydentátne ligandy – tvoria viac ako tri väzby, napríklad kyselina etyléndiamínotetraoctová (EDTA), schopná tvoriť až 6 väzieb s jedným centrálnym atómom
Namiesto latinského základu „dentátny“ (od dentis, zub) sa niekedy používajú slová funkčný, donorový alebo väzbový (napr. jednodonorové alebo dvojfunkčné ligandy).[1]
Ligandy, ktoré tvoria viac ako jednu väzbu, sa označujú ako chelačné činidlá. Komplexy, ktoré tvoria, sa potom označujú ako cheláty.[4]
Referencie
- ↑ a b c d e ligandy. In: BÍNA, Jaroslav. Malá encyklopédia chémie. Bratislava : Obzor, 1981. S. 429.
- ↑ koordinačná väzba. In: Encyclopaedia Beliana online
- ↑ koordinačné zlúčeniny. In: BÍNA, Jaroslav. Malá encyklopédia chémie. Bratislava : Obzor, 1981. S. 386.
- ↑ a b c d e ČERNÁK, Juraj. Úvod do koordinačnej chémie . Univerzita Jozefa Šafárika v Košiciach, 2011, . Dostupné online.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk