A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
- Nezamieňať s heslom tris(2-chlóretyl)fosforečnan.
| TCEP | |
 | |
 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C9H15O6P |
| Systematický názov | Kyselina 3,3′,3′′-fosfínetyltripropánová |
| Synonymá | Tris(2-karboxyetyl)fosfín |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 250,187 g/mol |
| Ďalšie informácie | |
| Číslo CAS | 51805-45-9 (chloridová soľ) |
| PubChem | 119411 |
| ChemSpider | 106653 |
| SMILES | OC(CCP(CCC(O)=O)CCC(O)=O)=O |
| 3D model (JSmol) | Interaktívny 3D model |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
TCEP je redukčné činidlo, ktoré sa často používa v biochémii a molekulárnej biológii.[1] Často sa pripravuje a používa v podobe chloridovej soli (TCEP-HCl). TCEP je rozpustný vo vode a dostupný v podobne stabilizovaného roztoku s neutrálnym pH alebo imobilizovaný na agarózovom géli, čo uľahčuje odstránenie činidla.
Reakcie
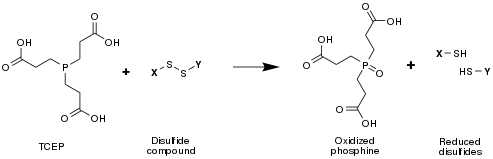
TCEP sa používa na redukciu disulfidických väzieb v bielkovinách:
Okrem toho bolo opísaných niekoľko ďalších reakcií:
- premena cysteínových reziduí na alanín v prítomnosti TCEP a vysokej teploty (90 °C)[2]
- pomalé štiepenie peptidových väzieb v bielkovinách u cysteínových reziduí pri miernych podmienkach (reakcia je pomalá, ale prebieha vo významnom množstve, po dvoch týždňoch skladovania pri 4 °C sa rozštiepilo až 40 % väzieb)[3]
Použitie
TCEP sa používa na štiepenie disulfidických väzieb, intra- i intermolekulárnych, v prípavných krokov pre gélovú elektroforézu.
V porovnaní s najbežnejšími činidlami používanými na tieto účely, ditiotreitolom a merkaptoetanolom, má TCEP niekoľko výhod: nemá žiadnu vôňu, je silnejším redukčným činidlom, oxiduje sa nevratne (produktom štiepenia sú dve voľné tiolové skupiny), je hydrofilnejší a odolnejší voči oxidácii na vzduchu.[4] Takisto neredukuje ióny kovov, ktoré sa používajú v imobilizovanej kovovej afinitnej chromatografii.
TCEP je obzvlášť užitočný pri označovaní cysteínových reziduí pomocou maleimidov. TCEP je schopný udržať voľné tiolové skupiny na cysteínoch a, na rozdiel od ditiotreitolu a merkaptoetanolu, nereaguje okamžite s maleimidom.[4] Boli však opísané i reakcie TCEP s maleimidom za istých podmienok.[5][6]
TCEP možno použiť i pri homogenizácii tkaniva pri izolácii RNA.[7]
TCEP má takisto tú výhodu, že pri použíti UV-Vis spektroskopie neabsorbuje v rozmedzí 250 až 285 nm,[8] na rozdiel od ditiotreitolu, takže ho možno použiť i pri stanoveniach prebiehajúcich pri týchto vlnových dĺžkach. Ditiotreitol v tomto rozmedzí vlnových dĺžok absorbuje stále viac a viac žiarenia, pretože sa v čase oxiduje rôznymi reakciami.
Biologický výskum
TCEP je dostupný od mnohých výrobcov v podobe chloridovej soli (s HCl). Po rozpustení TCEP-HCl vo vode vzniká kyslý roztok. Typicky sa pripravuje 0,5 M roztok TCEP-HCl a ten sa upravuje na pH blízko neutrálnemu pH, ktorý sa potom skladuje pri -20 °C.[9] TCEP je menej stabilný než fosfátové pufry.[9]
História
Redukcii biomolekúl pomocou trialkylfosfánov dlho nebola venovaná pozornosť, pretože historicky dostupné fosfíny mali veľmi nepríjemný zápach a/alebo neboli rozpustné vo vode.[10] V roku 1969 bol opísaný TCEP ako vo vode rozpustný trialkylfosfín bez zápachu pre biochemické použitie,[11] ale jeho potenciál bol ignorovaný po dobu niekoľkých dekád. V roku 1991 opísal Burns novú syntetickú cestu, ktorou ho možno pripraviť,[12] čo umožnilo bežnejšie použitie. Rovnako bol označený za „nové redukčné činidlo“ a začal sa bežne používať v 90. rokoch 20. storočia.[10]
Referencie
- ↑ Reductive cleavage of cystine disulfides with tributylphosphine. Methods Enzymol., 1977, s. 111–116. DOI: 10.1016/0076-6879(77)47012-5. PMID 927167.
- ↑ WANG, Zhouxi; REJTAR, Tomas; ZHOU, Zhaohui Sunny. Desulfurization of cysteine-containing peptides resulting from sample preparation for protein characterization by mass spectrometry. Rapid Communications in Mass Spectrometry (Wiley), 2010-01-04, s. 267–275. ISSN 0951-4198. DOI: 10.1002/rcm.4383.
- ↑ LIU, Peiran; O’MARA, Brian W.; WARRACK, Bethanne M.. A tris (2-carboxyethyl) phosphine (TCEP) related cleavage on cysteine-containing proteins. Journal of the American Society for Mass Spectrometry (American Chemical Society (ACS)), 2010-01-28, s. 837–844. ISSN 1044-0305. DOI: 10.1016/j.jasms.2010.01.016.
- ↑ a b TCEP technical information, from Interchim
- ↑ Reaction of Tris(2-carboxyethyl)phosphine (TCEP) with Maleimide and α-Haloacyl Groups: Anomalous Elution of TCEP by Gel Filtration. Anal. Biochem., 2002, s. 161–164. Dostupné online. DOI: 10.1006/abio.2000.4609. PMID 10860517.
- ↑ Thiol-reactive dyes for fluorescence labeling of proteomic samples. Electrophoresis, 2003, s. 2348–2358. DOI: 10.1002/elps.200305478. PMID 12874870.
- ↑ Tris(2-carboxyethyl)phosphine stabilization of RNA: comparison with dithiothreitol for use with nucleic acid and thiophosphoryl chemistry. Anal. Biochem., 2004, s. 137–143. DOI: 10.1016/j.ab.2003.10.019. PMID 14715294.
- ↑ KRȨŻEL, Artur; LATAJKA, Rafał; BUJACZ, Grzegorz D.. Coordination Properties of Tris(2-carboxyethyl)phosphine, a Newly Introduced Thiol Reductant, and Its Oxide. Inorganic Chemistry, 2003-03-01, roč. 42, čís. 6, s. 1994–2003. Dostupné online . ISSN 0020-1669. DOI: 10.1021/ic025969y. (po anglicky)
- ↑ a b Strategies for protein purification . Cytiva, . Dostupné online. Archivované 2023-02-24 z originálu.
- ↑ a b HAN, J.C.; HAN, G.Y.. A Procedure for Quantitative Determination of Tris(2-Carboxyethyl)phosphine, an Odorless Reducing Agent More Stable and Effective Than Dithiothreitol. Analytical Biochemistry (Elsevier BV), 1994, s. 5–10. ISSN 0003-2697. DOI: 10.1006/abio.1994.1290.
- ↑ LEVISON, M. E.; JOSEPHSON, A. S.; KIRSCHENBAUM, D. M.. Reduction of biological substances by water-soluble phosphines: Gamma-globulin (IgG). Experientia (Springer Science and Business Media LLC), 1969, s. 126–127. ISSN 0014-4754. DOI: 10.1007/bf01899076.
- ↑ BURNS, John A.; BUTLER, James C.; MORAN, John. Selective reduction of disulfides by tris(2-carboxyethyl)phosphine. The Journal of Organic Chemistry (American Chemical Society (ACS)), 1991, s. 2648–2650. ISSN 0022-3263. DOI: 10.1021/jo00008a014.
Pozri aj
- 2-merkaptoetanol (BME)
- Ditiotreitol (DTT)
- Ditiobutylamín (DTBA)
Zdroj
Tento článok je čiastočný alebo úplný preklad článku TCEP na anglickej Wikipédii.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk