
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
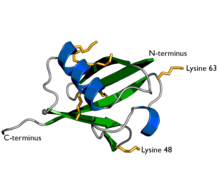
Ubiquitin či ubikvitin (z lat. ubique, všude) je malý globulární polypeptid o délce 76 aminokyselin a velikosti 8,6 kDa. Byl objeven Gideonem Goldsteinem roku 1975 a od té doby byl extenzivně studován[1]. Ubiquitin je přítomný ve všech eukaryotických buňkách, kde reguluje celou řadu funkcí jiných proteinů jako jejich buněčnou lokalizaci, stabilitu a rozklad v proteazomu, lyzozomu či ve vakuole. V určitých případech však také stimuluje endocytózu, vnitrobuněčný transport a podílí se na udržování struktury chromatinu (vazbou na histony)[2].
Ubiquitin reguluje funkci jiných proteinů procesem zvaným ubiquitinylace (příp. ubiquitinace, ubikvitinylace). Jedná se o kovalentní post-translační modifikaci proteinů, která hraje významnou roli ve stabilitě a degradaci proteinů, jejich buněčném umístění a aktivitě. Ubiquitin může být na protein navázán ve formě monomeru nebo polyubikquinových řetězců. Ubiquitin je u lidí kódován čtyřmi geny: UBB, UBC, RPS27A a UBA52[3].
Struktura
Ubiquitin je 76 aminokyselin dlouhý, kompaktní protein[4]. Jedná se o jeden z nejvíce konzervovaných eukaryotických proteinů[5].
Ubiquitin je exprimován ve formě prekurzorů: i) polyubiquitin složený z několika ubiquitinových jednotek v head-to-tail orientaci (u člověka kódován UBB, UBC) a ii) fúzní protein, kde je ubiquitin navázán zpravidla na ribozomální proteiny (u člověka RPS27A a UBA52), které jsou následně enzymaticky štěpeny na monomery ubiquitinu.
Aminokyselinová sekvence: MQIFVKTLTGKTITLEVEPSDTIENVKAKIQDKEGIPPDQQRLIFAGKQLEDGRTLSDYNIQKESTLHLVLRLRGG
Ubikvitinylace
Ubikvitinylace je typ post-translační modifikace proteinů, kdy je ubiquitin kovalentně připojen na substrátový protein. Nejčastěji se ubiquitin váže svým C-koncovým glycinem (G76) na lysin substrátu. Vzniká tak peptidická vazba mezi COO- skupinou ubiquitinu a ε-NH3+ lysinu substrátového proteinu [6].
Ubikvitinylace vyžaduje sled reakcí pro jsou nezbytné tři typy enzymů: ubiquitin-aktivující enzym (E1), ubiquitin-konjugující enzym (E2) a ubiquitin ligáza (E3).
- Aktivace (ATP závislá): Ubiquitin je aktivován dvou krokovou reakcí katalyzovanou E1 ubiquitin-aktivujícím enzymem. E1 váže ubiquitin a ATP a katalyzuje adenylaci C-koncového glycinu ubiquitinu za současného uvolnění pyrofosfátu. Následně je aktivovaný ubiquitin navázán thioesterovou vazbou na cystein E1 enzymu za uvolnění AMP.
- Konjugace: aktivovaný ubiquitin je dále přenesen trans-acetylací na E2 ubiquitin-konjugující enzym, který dále selektivně reaguje s E3 ubiquitin-ligázou. Zdá se, že při tvorbě polyubiquitinových řetězců je E2 enzym zodpovědný za rozhodnutí o jaký typ řetězce půjde a tím rozhoduje o osudu ubiquitinylovaných proteinů[7].
- Ligace: ligace může probíhat přímým přenosem ubiquitinu z E2 na substrát (v případě ubikvitinylace histonů) nebo pomocí E3 ubiquvitin-ligázy. Ubiquitin ligáza nejdřív váže substrátový protein a následně katalyzuje přenos ubiquitinu z E2 na substrát. E3 ubiquitin-ligáza je enzym zodpovědný za volbu substrátu, na který bude ubiquitin navázán[7][8].
Do dnešní doby bylo u člověka identifikováno pouze několik E1 enzymů, desítky E2 enzymů a stovky E3 ubiquitin-ligáz. Tyto počty reflektují hierarchické uspořádání a substrátovou specifitu daných enzymů.
Polyubiquitin
Ubiquitin se může vázat na jiné proteiny jako monomer nebo ve formě řetězců, kde jedna molekula ubiquitinu navázána na další. Ubiquitin obsahuje 7 lysinových zbytků (K6, K11, K27, K29, K33, K48, K63) a N-koncový methionin (M1) na které se může vázat další molekula ubiquitinu. Nejlépe charakterizované jsou K48, K63.
K48-vázané polyubiquitinové řetězce byly první identifikované[9]. K48-vázané řetězce jsou velmi kompaktní Tento typ řetězců hraje významnou roli v degradaci proteinů proteolýzou. Proteiny označené navázaným K48-polyubiquitinem mohou být rozeznány 26S proteazomem, který zapříčiní rozštěpení proteinů na peptidy. K48-polyubiquitinace hraje významnou roli v homeostázi a obratu proteinů. Minimální délka řetězce potřebná pro rozeznání proteazomem jsou 4 molekuly ubiquitinu[10].
K63-vázaný polyubiquitin neslouží ke značení proteinů k degradaci, naopak může zvyšovat jejich stabilitu a přispívat ke stabilitě signálních komplexů. Oproti K48-vázaným řetězcům jsou K63-vázané mnohem volnější.
M1-vázaný polyubiquitin (také lineární polyubiquitin) je další typ řetězce, který neslouží k označení pro degradaci. V tomto případě je ubiquitin vázán v head-to-tail orientaci, kde C-koncový glycin se váže přímo na N-koncový methionin. Přestože se původně myslelo, že M1-vázaný ubiquitin, podobně jako K48, slouží k proteinové degradaci[11], lineární ubiquitin se později ukázal jako nezbytný pro signalizaci přes NF-kB[12]. V současné době je známa pouze jedna E3 ligáza schopná tvořit lineární polyubiquitinové řetězce – linear ubiquitin chain assembly complex (LUBAC)[13][14].
Reference
- ↑ GOLDSTEIN, G; SCHEID, M; HAMMERLING, U. Isolation of a polypeptide that has lymphocyte-differentiating properties and is probably represented universally in living cells.. Proceedings of the National Academy of Sciences. 1975-01, roč. 72, čís. 1, s. 11–15. Dostupné online . ISSN 0027-8424. DOI 10.1073/pnas.72.1.11. PMID 1078892. (anglicky)
- ↑ ROBERT C. KING; WILLIAM D. STANSFIELD; PAMELA K. MULLIGAN. A Dictionary of Genetics, Seventh Edition. : Oxford University Press, 2006.
- ↑ KIMURA, Y.; TANAKA, K. Regulatory mechanisms involved in the control of ubiquitin homeostasis. Journal of Biochemistry. 2010-06-01, roč. 147, čís. 6, s. 793–798. Dostupné online . ISSN 0021-924X. DOI 10.1093/jb/mvq044. (anglicky)
- ↑ WILKINSON, K. D.; AUDHYA, T. K. Stimulation of ATP-dependent proteolysis requires ubiquitin with the COOH-terminal sequence Arg-Gly-Gly. The Journal of Biological Chemistry. 1981-09-10, roč. 256, čís. 17, s. 9235–9241. PMID: 6267067. Dostupné online . ISSN 0021-9258. PMID 6267067.
- ↑ VIJAY-KUMAR, Senadhi; BUGG, Charles E.; COOK, William J. Structure of ubiquitin refined at 1.8 Å resolution. Journal of Molecular Biology. 1987-04, roč. 194, čís. 3, s. 531–544. Dostupné online . DOI 10.1016/0022-2836(87)90679-6. (anglicky)
- ↑ HERSHKO, Avram; CIECHANOVER, Aaron. THE UBIQUITIN SYSTEM. Annual Review of Biochemistry. 1998-06, roč. 67, čís. 1, s. 425–479. Dostupné online . ISSN 0066-4154. DOI 10.1146/annurev.biochem.67.1.425. (anglicky)
- ↑ a b WIJK, Sjoerd J. L.; TIMMERS, H. T. Marc. The family of ubiquitin‐conjugating enzymes (E2s): deciding between life and death of proteins. The FASEB Journal. 2010-04, roč. 24, čís. 4, s. 981–993. Dostupné online . ISSN 0892-6638. DOI 10.1096/fj.09-136259. (anglicky)
- ↑ HERSHKO, Avram; CIECHANOVER, Aaron. THE UBIQUITIN SYSTEM FOR PROTEIN DEGRADATION. Annual Review of Biochemistry. 1992-06, roč. 61, čís. 1, s. 761–807. Dostupné online . ISSN 0066-4154. DOI 10.1146/annurev.bi.61.070192.003553. (anglicky)
- ↑ CHAU, Vincent; TOBIAS, John W.; BACHMAIR, Andreas. A Multiubiquitin Chain Is Confined to Specific Lysine in a Targeted Short-Lived Protein. Science. 1989-03-24, roč. 243, čís. 4898, s. 1576–1583. Dostupné online . ISSN 0036-8075. DOI 10.1126/science.2538923. (anglicky)
- ↑ THROWER, J. S. Recognition of the polyubiquitin proteolytic signal. The EMBO Journal. 2000-01-04, roč. 19, čís. 1, s. 94–102. Dostupné online . DOI 10.1093/emboj/19.1.94. PMID 10619848.
- ↑ NAKAMURA, Munehiro; TOKUNAGA, Fuminori; SAKATA, Shin-ichi. Mutual regulation of conventional protein kinase C and a ubiquitin ligase complex. Biochemical and Biophysical Research Communications. 2006-12-15, roč. 351, čís. 2, s. 340–347. Dostupné online . ISSN 0006-291X. DOI 10.1016/j.bbrc.2006.09.163. (anglicky)
- ↑ TOKUNAGA, Fuminori; SAKATA, Shin-ichi; SAEKI, Yasushi. Involvement of linear polyubiquitylation of NEMO in NF-κB activation. Nature Cell Biology. 2009-02, roč. 11, čís. 2, s. 123–132. Dostupné online . ISSN 1476-4679. DOI 10.1038/ncb1821. (anglicky)
- ↑ KIRISAKO, Takayoshi; KAMEI, Kiyoko; MURATA, Shigeo. A ubiquitin ligase complex assembles linear polyubiquitin chains. The EMBO Journal. 2006-10-18, roč. 25, čís. 20, s. 4877–4887. Dostupné online . ISSN 0261-4189. DOI 10.1038/sj.emboj.7601360. PMID 17006537.
- ↑ GERLACH, Björn; CORDIER, Stefanie M.; SCHMUKLE, Anna C. Linear ubiquitination prevents inflammation and regulates immune signalling. Nature. 2011-03, roč. 471, čís. 7340, s. 591–596. Dostupné online . ISSN 1476-4687. DOI 10.1038/nature09816. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu ubiquitin na Wikimedia Commons
Obrázky, zvuky či videa k tématu ubiquitin na Wikimedia Commons
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk
