A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Chlorid ortutný | |||||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||||
| Sumárny vzorec | Hg2Cl2 | ||||||||||||||||||||||||||||||||||
| Synonymá | Kalomel Dichlorid diortutný | ||||||||||||||||||||||||||||||||||
| Vzhľad | Biela kryštalická alebo práškovitá látka | ||||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||||
| Molekulová hmotnosť | 472,1 u | ||||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 472,086 g/mol | ||||||||||||||||||||||||||||||||||
| Teplota sublimácie | 383 °C | ||||||||||||||||||||||||||||||||||
| Trojný bod | 525 °C | ||||||||||||||||||||||||||||||||||
| Hustota | 7,150 g/cm3 | ||||||||||||||||||||||||||||||||||
| Rozpustnosť | vo vode: 0,2 mg/100 ml | ||||||||||||||||||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||||||||||||||||||
| Štandardná zlučovacia entalpia | -265 kJ/mol | ||||||||||||||||||||||||||||||||||
| Štandardná entropia | 196 J K−1 mol−1 | ||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||||
| Číslo CAS | 10112-91-1 | ||||||||||||||||||||||||||||||||||
| Číslo UN | 2025 | ||||||||||||||||||||||||||||||||||
| EINECS číslo | 233-307-5 | ||||||||||||||||||||||||||||||||||
| Číslo RTECS | OV8740000 | ||||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||||
Chlorid ortutný (Hg2Cl2) je anorganická zlúčenina chlóru a ortuti, v ktorej je oxidačné číslo ortuti I. V prírode sa nachádza ako zriedkavý minerál kalomel.[1]
Opis
Chlorid ortutný je hustá biela alebo žltkasto biela, pevná látka bez zápachu a vône. Chlorid ortutný býva súčasťou referenčnej elektródy v elektrochémii, takzvanej kalomelovej elektródy.[2][3]
Vlastnosti
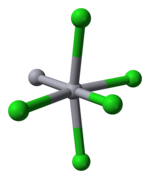
Ortuť je jedinečná pre svoju schopnosť ľahko vytvárať väzby typu M-M. Chlorid ortutný je lineárna molekula. Minerál kalomel kryštalizuje v tetragonálnej štruktúre, s priestorovým usporiadaním I4/m 2/m 2/m. Elementárna bunka z kryštálovej štruktúry je ukázaná nižšie:
Dĺžka väzby Hg-Hg je 253 pm (Hg-Hg v kove je 300 pm) a dĺžka väzby Hg-Cl v lineárnej štruktúre chloridu ortutného je 243 pm.[4] Celková koordinácia každého atómu ortute je oktaédrická, keďže okrem dvoch najbližších susedných atómov má každý atóm ortuti vo svojom okolí štyri atómy chlóru s väzbovou dĺžkou 321 pm. Vznikajúci oktaéder teda nie je pravidelný. V chloride ortutnom bola potvrdená i existencia dlhších polykatiónov ortute.[chýba zdroj
Výroba a reakcie
Chlorid ortutný sa vyrába reakciou elementárnej ortute s chloridom ortutnatým:[chýba zdroj
- Hg + HgCI2 → Hg2Cl2
Môže byť pripravený tiež pomocou zrážania v metatéznej reakcii vo vodnom roztoku dusičnanu ortutného s použitím rôznych zdrojov chloridového aniónu, vrátane NaCl alebo HCl:[chýba zdroj
- 2 HCl + Hg2(NO3)2 → Hg2Cl2 + 2 HNO3
Amoniak reaguje s chloridom ortutným, pričom dochádza k disproporcionácii:[chýba zdroj
- Hg2Cl2 + 2 NH3 → Hg + Hg(NH2)Cl + NH4Cl
Kalomelová elektróda
Chlorid ortutný sa používa vo veľkej miere v elektrochémii, s využitím jednoduchosti jeho oxidačno-redukčných reakcií. Kalomelová elektróda býva referenčnou elektródou, a to najmä v starších publikáciách. Počas posledných 50 rokov, bola nahradená argentochloridovou elektródou (Ag/AgCl). Aj keď sa ortuťové elektródy prestali používať vo veľkej miere, kvôli nebezpečnej povahe ortute, mnohý chemici veria, že sú stále lepšie a že nie sú nebezpečné, ak sú používané správne.[chýba zdroj Rozdiely v experimentálnych potenciáloch sa líšia len minimálne od hodnôt uvádzaných v literatúre. Ostatné typy elektród sa môžu líšiť v závislosti na podmienkach o 70 až 100 milivoltov.[chýba zdroj
Fotochémia
Chlorid ortutný sa po vystavení UV žiareniu rozloží na chlorid ortutnatý a elementárnu ortuť:
- Hg2Cl2 → HgCI2 + Hg
Proces tvorby ortute môže byť použitý pre výpočet počtu fotónov vo svetelnom zväzku technikou aktinometrie. Využitím svetelnej reakcie v prítomnosti chloridu ortutnatého a šťavelanu amónneho vzniká chlorid ortutný, chlorid amónny a oxid uhličitý:
- 2 HgCl2 + (NH4)2C2O4 + hν → Hg2Cl2(s) + 2 NH4Cl + 2 CO2
Táto konkrétna reakcia bola objavená J. M. Ederom (odtiaľ názov Ederova reakcia) v roku 1880 a opätovne overená W. E. Rosevaereom v roku 1929.[5]
Referencie
- ↑ Chisholm, Hugh, ed. (1910), „Calomel“, Encyclopædia Britannica (11th ed.), 5, Cambridge University Press, str. 59–60
- ↑ HOUSECROFT, Catherine E.; SHARPE, A. G.. Inorganic Chemistry. 3. vyd. : Pearson Education, 2008. Dostupné online. ISBN 978-0-13-175553-6. S. 222. (po anglicky)
- ↑ SKOOG, Douglas A.; HOLLER, F. James; NIEMAN, Timothy A.. Principles of Instrumental Analysis. 5th. vyd. : Saunders College Pub., 1998. ISBN 978-0-03-002078-0. S. 253–271.
- ↑ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 0-19-855370-6
- ↑ ROSEVEARE, W. E.. The X-Ray Photochemical Reaction between Potassium Oxalate and Mercuric Chloride. J. Am. Chem. Soc., 1930, s. 2612–2619. DOI: 10.1021/ja01370a005.
Pozri aj
Iný projekt
 Commons ponúka multimediálne súbory na tému Chlorid ortutný
Commons ponúka multimediálne súbory na tému Chlorid ortutný
Externé odkazy
- International Chemical Safety Card 0984
- National Pollutant Inventory - Mercury and compounds Fact Sheet
- NIOSH Pocket Guide to Chemical Hazards
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Mercury(I) chloride na anglickej Wikipédii.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
2,4,6-trinitrofenol
Anilín
Arzán
Bifenyl
Bromid kademnatý
Bromid ortutný
Bromid ortutnatý
Bromid zinočnatý
Chlorid arzenitý
Chlorid berýlnatý
Chlorid kademnatý
Chlorid kobaltnatý
Chlorid lantanitý
Chlorid mangánatý
Chlorid meďný
Chlorid meďnatý
Chlorid nikelnatý
Chlorid olovnatý
Chlorid ortutný
Chlorid ortutnatý
Chlorid sírnatý
Chlorid zinočnatý
Fosfán
Fosfid hlinitý
Fosfid zinočnatý
Glyfosát
Heptán
Hexán
Imazalil
Izooktán
Jodid antimonitý
Jodid kademnatý
Jodid meďný
Jodid olovnatý
Jodid ortutný
Jodid ortutnatý
Jodid sodný
Jodid strieborný
Jonón
Kumén
Kyanid draselný
Kyselina fluóroctová
Kyselina peroctová
Malachitová zeleň
Metántiol
Motorová nafta
Oktán
Oxid arzenitý
Oxid chloričitý
Oxid meďný
Oxid olovnato-olovičitý
Oxid zinočnatý
Pentachlórbenzén
Síran amónny
Síran meďnatý
Sírovodík
Selán
Strychnín
Sulfán
Tetrabrómbisfenol A
Tetrachlórmetán
Tiokyanatan meďný
Tiokyanatan strieborný
Tributylcín
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk